Autor: Dres. Lou F, Sarkaria I, Pietanza C, Travis W, Roh MS, Sica G, Healy D, Rusch V, Huang J. Ann Thorac Surgery 2013; 96(4): 1156-62
Los tumores carcinoides broncopulmonares son enfermedades malignas primarias relativamente raras en el pulmón, responsables por el 1% al 3% de los cánceres pulmonares resecados y por el 25% de todos los tumores carcinoides en el cuerpo [1-3]. Comparados con otros cánceres pulmonares no a células pequeñas (CPNCP), los tumores carcinoides, especialmente los carcinoides típicos, son menos agresivos, con pocas recidivas y muertes relacionadas con el cáncer, después del tratamiento. La resección quirúrgica sigue siendo el tratamiento de elección para los pacientes con carcinoides pulmonares diagnosticados [4]. A pesar de la naturaleza indolente de los tumores carcinoides, las tasas de recidiva post resección alcanzan un 5% para los carcinoides típicos y un 20% para los atípicos [5]. La vigilancia de rutina para la recurrencia ha sido aconsejada para los pacientes que han sido sometidos a procedimientos quirúrgicos para CPNCP [6]. La vigilancia estrecha puede llevar a la detección más temprana y tratamiento de las recidivas, mejorando los resultados globales.
Actualmente, la mayoría de las guías publicadas recomiendan la vigilancia de rutina con tomografía computada (TC) del tórax después de la resección quirúrgica para los CPNCP [6-9]. A causa de la falta de grandes estudios randomizados y prospectivos, las recomendaciones están basadas sobre un número limitado de series retrospectivas [10-12]. Un meta-análisis reciente encontró algún beneficio en la sobrevida para las estrategias de vigilancia más intensivas [13]. No obstante, esa diferencia puede ser confundida por las variaciones en los métodos de vigilancia y las poblaciones de pacientes. Reflejando su conducta menos agresiva, el pronóstico de los carcinoides broncopulmonares difiere de los otros subtipos de CPNCP. La intensidad del cuidado de seguimiento o incluso la necesidad de vigilancia, después del tratamiento de los tumores carcinoides, no han sido examinadas completamente.
Las recomendaciones apropiadas de seguimiento descansan sobre un entendimiento certero del riesgo de recidiva, incluyendo el momento, frecuencia y localización de las recaídas. El objetivo primario de este estudio fue examinar la detección y patrones de recidiva en pacientes sometidos a operaciones por tumores carcinoides pulmonares, que fueron seguidos con radiografías a intervalos programados.
Material y métodos
Los autores realizaron una revisión retrospectiva de una base de datos mantenida prospectivamente. Los pacientes que fueron sometidos a operaciones por carcinoides pulmonares primarios en el Memorial Sloan-Kettering Cancer Center (MSKCC) entre 1993 y 2010, fueron identificados en la base de datos; 345 casos únicos fueron encontrados. Aquellos con antecedentes de cáncer pulmonar (n = 7) y resección efectuada en otras instituciones (n = 1), fueron excluidos. Un total de 337 pacientes fueron incluidos en este estudio. Las características basales y de tratamiento, tales como el estadio anatomopatológico, variables demográficas, estadio clínico y detalles de la resección, fueron extraídos de la base de datos. Los registros médicos electrónicos fueron revisados para la información de seguimiento, incluyendo el estatus de recidiva, tratamientos para la recaída y métodos de detección. El estatus de recidiva fue censado en la última cita clínica de seguimiento o por comunicación documentada. El estatus vital fue confirmado por el Social Security Death Index. El seguimiento alejado fue conducido hasta junio de 2011. La estadificación anatomopatológica fue realizada de acuerdo con le séptima edición del manual de estadificación del American Joint Committee on Cancer [14].
La evaluación preoperatoria de la extensión de la enfermedad incluyó TC del tórax y abdomen superior. La estadificación adicional, incluyendo tomografía de emisión de positrones (TEP), mediastinoscopía o exploración con octreotide, fue realizada a discreción de los clínicos. Siempre que fue posible, se realizaron las resecciones anatómicas en lugar de resecciones en cuña. En general, la disección ganglionar linfática mediastinal sistemática fue efectuada rutinariamente, como parte de la resección anatómica. Todos los especímenes anatomopatológicos fueron revisados por un único patólogo (W.D.T). Los tumores fueron clasificados como carcinoides típicos o atípicos, de acuerdo con las guías de clasificación 2004 de la Organización Mundial de la Salud [15]. Los pacientes sólo con tumorlets carcinoides no fueron incluidos en el estudio.
Los pacientes fueron seguidos por su cirujano primario, un oncólogo, o personal de enfermería especializado en supervivencia torácica. El método preciso de seguimiento fue dejado a discreción de los médicos. Más comúnmente, se realizaron cada 6 a 12 meses, exámenes físicos y radiografías de tórax. Los diagnósticos de recidivas fueron adjudicados por biopsias o estudios por imágenes. Las recidivas locorregionales fueron definidas como lesiones nuevas en el sitio de resección, incluyendo la línea de engrampado o muñón bronquial, o en los ganglios linfáticos hiliares ipsilaterales o mediastinales. Las metástasis a distancia fueron definidas como tumores comprometiendo todas las otras localizaciones, incluyendo derrames pleurales y pericárdicos. Este estudio fue aprobado por el comité de revisión institucional del MSKCC.
Análisis estadístico
Se usó el programa SAS, versión 9.3 (SAS Institute, Cary, NC) para realizar todos los análisis. El momento de la recidiva fue calculado desde la fecha de la operación hasta el diagnóstico de la recurrencia por estudios anatomopatológicos o de imágenes. Los datos resumidos son presentados como proporciones y media ± desvío estándar (DE). El método de Kaplan-Meier fue usado para resumir la sobrevida y el momento de la recaída. La prueba no paramétrica de log-rank fue usada para realizar la comparación entre los grupos. Todas las pruebas fueron de dos lados, con un valor α preestablecido de 0,05.
Resultados
Características basalesUn total de 337 pacientes fueron estudiados. El tempo medio de seguimiento para aquellos que permanecieron vivos y sin recaída, fue de 42 meses (rango, 0-197 meses). Las variables demográficas son resumidas en la Tabla 1. Para señalar: poco más de la mitad (142 [52%]) de los tumores carcinoides pulmonares fueron primero descubiertos incidentalmente. La mayoría de los pacientes restantes (42%) presentó primero síntomas. Las características del cáncer y del tratamiento se presentan en la Tabla 2. La quimioterapia de inducción fue administrada a 5 pacientes. La mayoría de los pacientes (82%) fue sometida a resección por enfermedad en estadio I. Los carcinoides típicos fueron identificados en el análisis anatomopatológico en más del 86% de los pacientes. La lobectomía fue el procedimiento más comúnmente realizado (62%), seguida por la resección en cuña (19%) y la bilobectomia (9%). La resección en manguito fue realizada en 19 pacientes. Concordante con el estadio temprano y la naturaleza indolente de los tumores carcinoides, la vasta mayoría de los pacientes (219 [81%]) no fue sometida a terapia adyuvante adicional después de la cirugía.
• TABLA 1: Variables demográficas
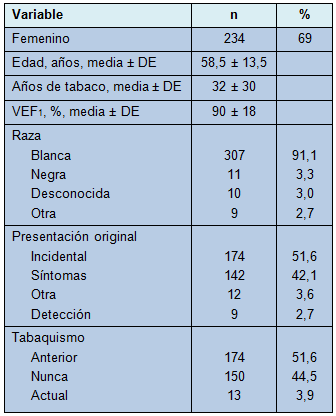
• TABLA 2: Características del cáncer y tratamiento
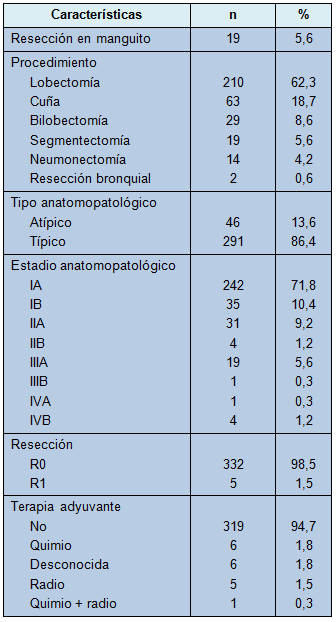 Detección de la recidiva
Detección de la recidiva
Durante el período de seguimiento, 21 pacientes experimentaron recidivas: 17 con metástasis a distancia (81%), 1 con enfermedad locorregional solamente (5%) y 3 con recaída a distancia y local (14%). En 1 paciente, un segundo cáncer pulmonar primario se desarrolló en un lóbulo contralateral. Los síntomas llevaron al diagnóstico de la recaída de la enfermedad en 7 pacientes (33%), y la TC de vigilancia en el seguimiento llevó al diagnóstico de sólo cinco casos de recidiva (23%) y un caso de segundo tumor primario de pulmón (Tabla 3). Los síntomas de recidiva incluyeron dolor óseo (n = 3), hemoptisis (n = 1), dificultad respiratoria aguda (n = 1), dolor abdominal (n = 1) y debilidad/pérdida de peso (n = 1). Para señalar: un número significativo de recidivas fue diagnosticado incidentalmente (8 [38%]). Los pacientes en ese grupo tuvieron estudios por dolencias no relacionadas, tales como tos no específica, mareos e hipercoagulabilidad y por atención de seguimiento después de otro cáncer y accidentes automotores. En 1 paciente, se encontró una metástasis hepática durante una colecistectomía laparoscópica por colelitiasis, aunque las TC de tórax y abdomen superior de vigilancia fueron negativas 2 meses antes.
• TABLA 3: Detección de la recidiva en 21 pacientes
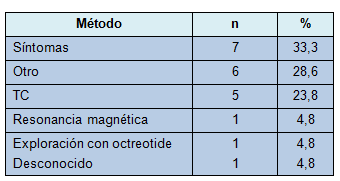 Patrones de recidiva y tratamientos
Patrones de recidiva y tratamientos
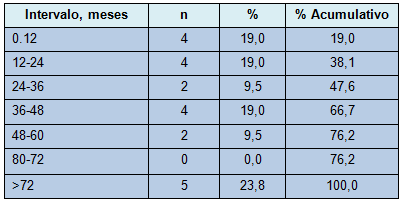
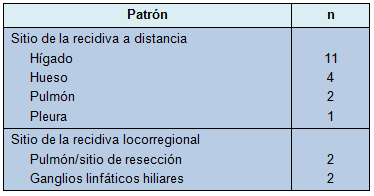
Entre aproximadamente el 10% y el 19% de las recidivas ocurrieron durante cada año, después de la operación, en los primeros 5 años (Tabla 4). En los pacientes con evidencia de metástasis a distancia, el hígado (n = 11) y el hueso (n = 4), fueron los sitios más comunes de recaída (Tabla 5). Se encontró que los pacientes con recidiva locorregional tenían enfermedad alrededor de los sitios de resección (n = 2) y en los ganglios linfáticos ipsilaterales (n = 2). El paciente sólo con recidiva local, tenía enfermedad en lo ganglios linfáticos mediastinales. Los tratamientos más comunes después del diagnóstico de recidiva fueron octreotide (n = 5) y quimioterapia (n = 4). Tres pacientes recibieron embolización hepática por metástasis en el hígado. El paciente con un segundo cáncer primario pulmonar fue sometido a una resección en cuña del nuevo tumor.
• TABLA 4: Proporción de recidivas
• TABLA 5: Patrón de recidiva en 21 pacientes
 Comparado con los pacientes que tenían carcinoides atípicos, aquellos con carcinoides típicos tuvieron una probabilidad significativamente más baja de recidiva (p < 0,0001). Además, el compromiso ganglionar linfático aumentó la tasa de recidiva para ambos tipos anatomopatológicos (p < 0,0001). De los 46 pacientes con carcinoides atípicos, 12 experimentaron recidivas (26%). Tres pacientes tenían enfermedad tanto locorregional como a distancia, mientras que 8 tenían metástasis a distancia solamente y 1 experimentó enfermedad localizada en los ganglios linfáticos mediastinales. La mediana del tiempo para la recidiva fue de 22 meses (rango, 2-83 meses). En contraste, 9 de los 291 pacientes (3%) con carcinoides típicos tuvieron diagnóstico de recidiva. Asimismo, sólo 6 de los 268 pacientes (2%) con carcinoides típicos con ganglios negativos experimentaron recidivas. Todas las recidivas de los carcinoides típicos fueron metástasis a distancia. La mediana del tiempo hasta la recidiva fue de 50 meses (rango, 9-141 meses), más larga que para las recidivas de los carcinoides atípicos. Cuando se compararon las resecciones en cuña con las resecciones anatómicas, no hubo diferencia en las recidivas (p = 0,98). Eso fue cierto aún cuando el tipo anatomopatológico y el estatus ganglionar fueron controlados.
Comparado con los pacientes que tenían carcinoides atípicos, aquellos con carcinoides típicos tuvieron una probabilidad significativamente más baja de recidiva (p < 0,0001). Además, el compromiso ganglionar linfático aumentó la tasa de recidiva para ambos tipos anatomopatológicos (p < 0,0001). De los 46 pacientes con carcinoides atípicos, 12 experimentaron recidivas (26%). Tres pacientes tenían enfermedad tanto locorregional como a distancia, mientras que 8 tenían metástasis a distancia solamente y 1 experimentó enfermedad localizada en los ganglios linfáticos mediastinales. La mediana del tiempo para la recidiva fue de 22 meses (rango, 2-83 meses). En contraste, 9 de los 291 pacientes (3%) con carcinoides típicos tuvieron diagnóstico de recidiva. Asimismo, sólo 6 de los 268 pacientes (2%) con carcinoides típicos con ganglios negativos experimentaron recidivas. Todas las recidivas de los carcinoides típicos fueron metástasis a distancia. La mediana del tiempo hasta la recidiva fue de 50 meses (rango, 9-141 meses), más larga que para las recidivas de los carcinoides atípicos. Cuando se compararon las resecciones en cuña con las resecciones anatómicas, no hubo diferencia en las recidivas (p = 0,98). Eso fue cierto aún cuando el tipo anatomopatológico y el estatus ganglionar fueron controlados.
Comentario
Los tumores carcinoides broncopulmonares son cánceres pulmonares primarios raros y se conoce que son más indolentes que otros CPNCP. Sin embargo, hasta el 20% de los pacientes con carcinoides atípicos puede experimentar recidivas [5]. La detección más temprana de la recaída puede conducir a un rápido tratamiento y mejora de la sobrevida. Actualmente, el patrón de recidiva y la eficacia de la vigilancia de rutina no han sido examinados en sobrevivientes de tumores carcinoides pulmonares, hasta donde llega el conocimiento de los autores de este trabajo. En este estudio, los autores examinaron las fallas del tratamiento y de los métodos de detección, después de la resección quirúrgica de los cánceres carcinoides pulmonares primarios. Los pacientes fueron sometidos a vigilancia de rutina durante el seguimiento, a discreción de los médicos. La mayoría de los regímenes de seguimiento involucran visitas programadas al consultorio y TC de tórax y abdomen superior o radiografía de tórax. Los autores observaron tasas más altas de recidiva y disminución de la sobrevida entre los pacientes con tipo anatomopatológico atípico y compromiso positivo de los ganglios linfáticos La mayoría de las recaídas involucra metástasis a sitios distantes. Sólo el 2% de los pacientes con carcinoides típicos y ganglios linfáticos negativos experimentó recidivas. De importancia, las imágenes de vigilancia de rutina no detectaron una proporción significativa de las recidivas.
Actualmente, existe limitada evidencia sobre el efecto de los programas de vigilancia en la sobrevida y en los resultados orientados al paciente, después de la resección quirúrgica por CPNCP. Sin embargo, la mayoría de las guías prácticas publicadas recomiendan un seguimiento a largo plazo de rutina, que combina visitas al consultorio con estudios programados [6-9,16]. Las recomendaciones para el seguimiento post resección están basadas en series retrospectivas de vigilancia y en ensayos prospectivos randomizados de detección con TC en individuos con alto riesgo. Varias series han investigado los patrones de recidiva y la eficacia de los estudios por imágenes de rutina en CPNCP [10-12,17,18]. En muchos estudios, la TC de tórax a intervalo cercano detectó la mayoría de los segundos cánceres pulmonares primarios, durante los estadios tempranos asintomáticos. Sobre la base de la tasa alta de enfermedades malignas pulmonares metacrónicas y el poder de detección de la TC de rutina, la TC de vigilancia podría ser probablemente beneficiosa para los sobrevivientes de cáncer pulmonar. Recientemente, las guías de la American Association for Thoracic Surgery sobre detección y vigilancia del cáncer de pulmón, recomendaron que los sobrevivientes a largo plazo de cáncer pulmonar deberían ser sometidos anualmente a una TC de baja dosis, para detectar nuevas malignidades pulmonares primarias [6].
Varios aspectos de la vigilancia no han sido abordados, hasta donde llega el conocimiento de los autores del este trabajo. Primero, no está claro si la detección y tratamiento más tempranos de la recidiva mejoran necesariamente la sobrevida a largo plazo. Segundo, los efectos negativos de las imágenes de rutina no han sido investigados a gran escala. Una revisión sistemática conducida por Bach y col. [19], analizó 591 citas sobre los beneficios y peligros de la TC de baja dosis. Aunque aproximadamente sólo el 1% de los pacientes tuvo diagnóstico de cáncer pulmonar, aproximadamente el 20% de los pacientes, a través de todos los estudios, tuvo resultados positivos de las pruebas de detección, requiriendo estudios adicionales. Los autores concluyeron que la TC de baja dosis puede ser beneficiosa para los pacientes con riesgo alto, pero que los peligros potenciales de la detección deben ser investigados y factoreados dentro de futuros protocolos de detección.
Las guías actuales para la vigilancia están basadas en series retrospectivas de pacientes tratados por CPNCP, mayormente adenocarcinoma y carcinoma de células escamosas. Comparado con los tipos histológicos más comunes de cáncer de pulmón, los carcinoides difieren en su conducta, tratamiento y pronóstico global. Dada la naturaleza indolente de los carcinoides típicos, se ha sugerido que, en esa cohorte, las resecciones sublobares pueden producir resultados de sobrevida que son similares a aquellos para las resecciones lobares [20]. El rol de la vigilancia en los sobrevivientes de cáncer carcinoide debería ser examinado separadamente del de los pacientes con tipos más agresivos de cáncer de pulmón [21].
En concordancia con series previas sobre tumores carcinoides, los autores de este trabajo hallaron que el carcinoide atípico y el estatus ganglionar linfático predicen tasas más altas de recidiva después de la resección quirúrgica [21-25]. No obstante, a pesar del seguimiento regular después de la operación, la TC de tórax y abdomen superior de rutina, realizada relativamente de manera pobre, detectó sólo 1 de 4 recaídas. La razón para esa tasa baja de detección de la TC de vigilancia puede estar relacionada con la modalidad de imagen y el patrón de recidiva. La radiología del tórax puede no ser lo suficientemente sensible para detectar pequeñas recidivas intratorácicas. Además, las TC realizadas sin contraste endovenoso pueden omitir metástasis hepáticas o adrenales. Dado que la mayoría de las recaídas fueron metástasis a distancia, los estudios por imágenes restringidos al tórax, fallan en detectar cualquier recidiva extratorácica.
Además de la localización, un régimen racional de vigilancia debe tomar también en cuenta el momento de la recidiva y la probabilidad de eventos. El tiempo más largo para la recidiva en esta serie fue mayor de 11 años. Otras series han reportado recidivas a largo plazo hasta 20 años después de la operación [23,26]. A causa de esos hallazgos, algunos autores recomendaron que el seguimiento debe continuar por al menos 20 años [7]. Sin embargo, si las recidivas son raras, la utilidad de las imágenes repetidas durante ese período extendido, es cuestionable.
Otra consideración importante para diseñar un programa de vigilancia apropiado es contrapesar los beneficios de la vigilancia con los potenciales efectos negativos, teniendo en mente la señal de precaución pronunciada por Bach y col. [19], en su revisión sistemática de la TC de detección. Los riesgos potenciales, además de la exposición a la radiación, incluyen ansiedad aumentada del paciente y resultados falso positivos que pueden llevar a pruebas ulteriores, costos amentados, morbilidad aumentada e incluso aumento de la mortalidad por procedimientos invasivos innecesarios. En una serie previa sobre vigilancia en pacientes tratados por CPNCP en estadio temprano, los autores hallaron que un cuarto de los pacientes requirió pruebas adicionales a causa de resultados falso positivos durante la vigilancia [27]. Aunque es difícil evaluar el balance de riesgos y beneficios de la vigilancia en pacientes con tumores carcinoides en un estudio retrospectivo, los pacientes con el riesgo más bajo de recidiva son los menos propensos a beneficiarse con la vigilancia. La relativa inefectividad de la TC de vigilancia para la detección de las recidivas y el hecho de que un cuarto de las recidivas ocurre después de los 6 años, eleva las cuestiones sobre la costo-efectividad de la vigilancia sistemática con imágenes, en el seguimiento de los pacientes con carcinoides.
Sobre la base de la experiencia de la institución en donde se desempeñan los autores del presente estudio, los pacientes con tumores carcinoides completamente resecados y con ganglios negativos, pueden no justificar una vigilancia a largo plazo, dada la tasa muy baja de recidiva en esa cohorte. No obstante, la vigilancia de rutina con TC debería ser realizada en los pacientes tratados por carcinoide atípico o carcinoide típico con compromiso positivo de los ganglios linfáticos. Dado que la TC es más sensible que la radiología de tórax, debería ser usada como la modalidad primaria de vigilancia. La TC de intervalo debería incluir el tórax y el abdomen superior, incluyendo el hígado y las adrenales, y ser realizada con medio de contraste, para ayudar en la evaluación de los órganos sólidos y ganglios mediastinales. Puesto que el número de recidivas diagnosticadas permanece constante en el tiempo, las TC de vigilancia deberían realizarse cada 12 meses.
La vigilancia de las recidivas después de la resección quirúrgica sigue siendo un aspecto importante de la atención del cáncer, con un impacto significativo en la sobrevida, calidad de vida y costos por la atención médica. Los estudios futuros sobre la vigilancia para la recidiva de los carcinoides pulmonares deberían enfocarse sobre varios aspectos específicos de la naturaleza de la enfermedad. Primero, dada la rareza del cáncer carcinoide pulmonar comparado con otros CPNCP, debería hacerse un esfuerzo para estudiar datos agrupados de múltiples instituciones en una escala internacional. La mayoría de las recidivas de los tumores carcinoides son metástasis a distancia. La vigilancia limitada al tórax o incluso al abdomen superior, puede no ser efectiva para detectar la recaída en otras áreas del cuerpo. La efectividad de otras modalidades de imágenes sistemáticamente orientadas, tales como la TEP/TC y exámenes con octreotide, queda por determinarse y es una cuestión abierta para investigación adicional. Finalmente, son necesarios grandes ensayos prospectivos y randomizados, para estudiar el efecto de la vigilancia en la sobrevida, costos y calidad de vida.
Limitaciones
Este estudio está limitado por su naturaleza retrospectiva y el enfoque sobre pacientes tratados en una única institución. Aunque la mayoría de los pacientes fue sometida a vigilancia de rutina con TC, puede haber variabilidad en sus regímenes de seguimiento, dado que no se especificó un protocolo prospectivo. Como en todo estudio retrospectivo, este análisis no fue diseñado para evaluar el efecto de las imágenes de vigilancia sobre la calidad de vida y la sobrevida. No puede o debe establecerse ninguna conclusión sobre el impacto de las imágenes de vigilancia en la sobrevida, porque ese no fue el foco de este estudio.
Resumen
Después de la operación por tumores carcinoides pulmonares, las imágenes de vigilancia fallaron para detectar la mayoría de las recaídas. Las recidivas se desarrollaron raramente en los pacientes con tumores carcinoides típicos con ganglios linfáticos negativos. Debido al bajo riesgo de recidiva y a la poco clara eficacia de las imágenes de vigilancia, las mismas hechas rutinariamente pueden no estar justificadas en esa cohorte. Los estudios futuros deberían enfocarse sobre los efectos de la vigilancia en la sobrevida y resultados orientados al paciente y sobre las estrategias alternativas para el seguimiento.
♦ Comentario y resumen objetivo: Dr. Rodolfo D. Altrudi
Los tumores carcinoides broncopulmonares son enfermedades malignas primarias relativamente raras en el pulmón, responsables por el 1% al 3% de los cánceres pulmonares resecados y por el 25% de todos los tumores carcinoides en el cuerpo [1-3]. Comparados con otros cánceres pulmonares no a células pequeñas (CPNCP), los tumores carcinoides, especialmente los carcinoides típicos, son menos agresivos, con pocas recidivas y muertes relacionadas con el cáncer, después del tratamiento. La resección quirúrgica sigue siendo el tratamiento de elección para los pacientes con carcinoides pulmonares diagnosticados [4]. A pesar de la naturaleza indolente de los tumores carcinoides, las tasas de recidiva post resección alcanzan un 5% para los carcinoides típicos y un 20% para los atípicos [5]. La vigilancia de rutina para la recurrencia ha sido aconsejada para los pacientes que han sido sometidos a procedimientos quirúrgicos para CPNCP [6]. La vigilancia estrecha puede llevar a la detección más temprana y tratamiento de las recidivas, mejorando los resultados globales.
Actualmente, la mayoría de las guías publicadas recomiendan la vigilancia de rutina con tomografía computada (TC) del tórax después de la resección quirúrgica para los CPNCP [6-9]. A causa de la falta de grandes estudios randomizados y prospectivos, las recomendaciones están basadas sobre un número limitado de series retrospectivas [10-12]. Un meta-análisis reciente encontró algún beneficio en la sobrevida para las estrategias de vigilancia más intensivas [13]. No obstante, esa diferencia puede ser confundida por las variaciones en los métodos de vigilancia y las poblaciones de pacientes. Reflejando su conducta menos agresiva, el pronóstico de los carcinoides broncopulmonares difiere de los otros subtipos de CPNCP. La intensidad del cuidado de seguimiento o incluso la necesidad de vigilancia, después del tratamiento de los tumores carcinoides, no han sido examinadas completamente.
Las recomendaciones apropiadas de seguimiento descansan sobre un entendimiento certero del riesgo de recidiva, incluyendo el momento, frecuencia y localización de las recaídas. El objetivo primario de este estudio fue examinar la detección y patrones de recidiva en pacientes sometidos a operaciones por tumores carcinoides pulmonares, que fueron seguidos con radiografías a intervalos programados.
Material y métodos
Los autores realizaron una revisión retrospectiva de una base de datos mantenida prospectivamente. Los pacientes que fueron sometidos a operaciones por carcinoides pulmonares primarios en el Memorial Sloan-Kettering Cancer Center (MSKCC) entre 1993 y 2010, fueron identificados en la base de datos; 345 casos únicos fueron encontrados. Aquellos con antecedentes de cáncer pulmonar (n = 7) y resección efectuada en otras instituciones (n = 1), fueron excluidos. Un total de 337 pacientes fueron incluidos en este estudio. Las características basales y de tratamiento, tales como el estadio anatomopatológico, variables demográficas, estadio clínico y detalles de la resección, fueron extraídos de la base de datos. Los registros médicos electrónicos fueron revisados para la información de seguimiento, incluyendo el estatus de recidiva, tratamientos para la recaída y métodos de detección. El estatus de recidiva fue censado en la última cita clínica de seguimiento o por comunicación documentada. El estatus vital fue confirmado por el Social Security Death Index. El seguimiento alejado fue conducido hasta junio de 2011. La estadificación anatomopatológica fue realizada de acuerdo con le séptima edición del manual de estadificación del American Joint Committee on Cancer [14].
La evaluación preoperatoria de la extensión de la enfermedad incluyó TC del tórax y abdomen superior. La estadificación adicional, incluyendo tomografía de emisión de positrones (TEP), mediastinoscopía o exploración con octreotide, fue realizada a discreción de los clínicos. Siempre que fue posible, se realizaron las resecciones anatómicas en lugar de resecciones en cuña. En general, la disección ganglionar linfática mediastinal sistemática fue efectuada rutinariamente, como parte de la resección anatómica. Todos los especímenes anatomopatológicos fueron revisados por un único patólogo (W.D.T). Los tumores fueron clasificados como carcinoides típicos o atípicos, de acuerdo con las guías de clasificación 2004 de la Organización Mundial de la Salud [15]. Los pacientes sólo con tumorlets carcinoides no fueron incluidos en el estudio.
Los pacientes fueron seguidos por su cirujano primario, un oncólogo, o personal de enfermería especializado en supervivencia torácica. El método preciso de seguimiento fue dejado a discreción de los médicos. Más comúnmente, se realizaron cada 6 a 12 meses, exámenes físicos y radiografías de tórax. Los diagnósticos de recidivas fueron adjudicados por biopsias o estudios por imágenes. Las recidivas locorregionales fueron definidas como lesiones nuevas en el sitio de resección, incluyendo la línea de engrampado o muñón bronquial, o en los ganglios linfáticos hiliares ipsilaterales o mediastinales. Las metástasis a distancia fueron definidas como tumores comprometiendo todas las otras localizaciones, incluyendo derrames pleurales y pericárdicos. Este estudio fue aprobado por el comité de revisión institucional del MSKCC.
Análisis estadístico
Se usó el programa SAS, versión 9.3 (SAS Institute, Cary, NC) para realizar todos los análisis. El momento de la recidiva fue calculado desde la fecha de la operación hasta el diagnóstico de la recurrencia por estudios anatomopatológicos o de imágenes. Los datos resumidos son presentados como proporciones y media ± desvío estándar (DE). El método de Kaplan-Meier fue usado para resumir la sobrevida y el momento de la recaída. La prueba no paramétrica de log-rank fue usada para realizar la comparación entre los grupos. Todas las pruebas fueron de dos lados, con un valor α preestablecido de 0,05.
Resultados
Características basalesUn total de 337 pacientes fueron estudiados. El tempo medio de seguimiento para aquellos que permanecieron vivos y sin recaída, fue de 42 meses (rango, 0-197 meses). Las variables demográficas son resumidas en la Tabla 1. Para señalar: poco más de la mitad (142 [52%]) de los tumores carcinoides pulmonares fueron primero descubiertos incidentalmente. La mayoría de los pacientes restantes (42%) presentó primero síntomas. Las características del cáncer y del tratamiento se presentan en la Tabla 2. La quimioterapia de inducción fue administrada a 5 pacientes. La mayoría de los pacientes (82%) fue sometida a resección por enfermedad en estadio I. Los carcinoides típicos fueron identificados en el análisis anatomopatológico en más del 86% de los pacientes. La lobectomía fue el procedimiento más comúnmente realizado (62%), seguida por la resección en cuña (19%) y la bilobectomia (9%). La resección en manguito fue realizada en 19 pacientes. Concordante con el estadio temprano y la naturaleza indolente de los tumores carcinoides, la vasta mayoría de los pacientes (219 [81%]) no fue sometida a terapia adyuvante adicional después de la cirugía.
• TABLA 1: Variables demográficas


Durante el período de seguimiento, 21 pacientes experimentaron recidivas: 17 con metástasis a distancia (81%), 1 con enfermedad locorregional solamente (5%) y 3 con recaída a distancia y local (14%). En 1 paciente, un segundo cáncer pulmonar primario se desarrolló en un lóbulo contralateral. Los síntomas llevaron al diagnóstico de la recaída de la enfermedad en 7 pacientes (33%), y la TC de vigilancia en el seguimiento llevó al diagnóstico de sólo cinco casos de recidiva (23%) y un caso de segundo tumor primario de pulmón (Tabla 3). Los síntomas de recidiva incluyeron dolor óseo (n = 3), hemoptisis (n = 1), dificultad respiratoria aguda (n = 1), dolor abdominal (n = 1) y debilidad/pérdida de peso (n = 1). Para señalar: un número significativo de recidivas fue diagnosticado incidentalmente (8 [38%]). Los pacientes en ese grupo tuvieron estudios por dolencias no relacionadas, tales como tos no específica, mareos e hipercoagulabilidad y por atención de seguimiento después de otro cáncer y accidentes automotores. En 1 paciente, se encontró una metástasis hepática durante una colecistectomía laparoscópica por colelitiasis, aunque las TC de tórax y abdomen superior de vigilancia fueron negativas 2 meses antes.
• TABLA 3: Detección de la recidiva en 21 pacientes

Entre aproximadamente el 10% y el 19% de las recidivas ocurrieron durante cada año, después de la operación, en los primeros 5 años (Tabla 4). En los pacientes con evidencia de metástasis a distancia, el hígado (n = 11) y el hueso (n = 4), fueron los sitios más comunes de recaída (Tabla 5). Se encontró que los pacientes con recidiva locorregional tenían enfermedad alrededor de los sitios de resección (n = 2) y en los ganglios linfáticos ipsilaterales (n = 2). El paciente sólo con recidiva local, tenía enfermedad en lo ganglios linfáticos mediastinales. Los tratamientos más comunes después del diagnóstico de recidiva fueron octreotide (n = 5) y quimioterapia (n = 4). Tres pacientes recibieron embolización hepática por metástasis en el hígado. El paciente con un segundo cáncer primario pulmonar fue sometido a una resección en cuña del nuevo tumor.
• TABLA 4: Proporción de recidivas

• TABLA 5: Patrón de recidiva en 21 pacientes

Comentario
Los tumores carcinoides broncopulmonares son cánceres pulmonares primarios raros y se conoce que son más indolentes que otros CPNCP. Sin embargo, hasta el 20% de los pacientes con carcinoides atípicos puede experimentar recidivas [5]. La detección más temprana de la recaída puede conducir a un rápido tratamiento y mejora de la sobrevida. Actualmente, el patrón de recidiva y la eficacia de la vigilancia de rutina no han sido examinados en sobrevivientes de tumores carcinoides pulmonares, hasta donde llega el conocimiento de los autores de este trabajo. En este estudio, los autores examinaron las fallas del tratamiento y de los métodos de detección, después de la resección quirúrgica de los cánceres carcinoides pulmonares primarios. Los pacientes fueron sometidos a vigilancia de rutina durante el seguimiento, a discreción de los médicos. La mayoría de los regímenes de seguimiento involucran visitas programadas al consultorio y TC de tórax y abdomen superior o radiografía de tórax. Los autores observaron tasas más altas de recidiva y disminución de la sobrevida entre los pacientes con tipo anatomopatológico atípico y compromiso positivo de los ganglios linfáticos La mayoría de las recaídas involucra metástasis a sitios distantes. Sólo el 2% de los pacientes con carcinoides típicos y ganglios linfáticos negativos experimentó recidivas. De importancia, las imágenes de vigilancia de rutina no detectaron una proporción significativa de las recidivas.
Actualmente, existe limitada evidencia sobre el efecto de los programas de vigilancia en la sobrevida y en los resultados orientados al paciente, después de la resección quirúrgica por CPNCP. Sin embargo, la mayoría de las guías prácticas publicadas recomiendan un seguimiento a largo plazo de rutina, que combina visitas al consultorio con estudios programados [6-9,16]. Las recomendaciones para el seguimiento post resección están basadas en series retrospectivas de vigilancia y en ensayos prospectivos randomizados de detección con TC en individuos con alto riesgo. Varias series han investigado los patrones de recidiva y la eficacia de los estudios por imágenes de rutina en CPNCP [10-12,17,18]. En muchos estudios, la TC de tórax a intervalo cercano detectó la mayoría de los segundos cánceres pulmonares primarios, durante los estadios tempranos asintomáticos. Sobre la base de la tasa alta de enfermedades malignas pulmonares metacrónicas y el poder de detección de la TC de rutina, la TC de vigilancia podría ser probablemente beneficiosa para los sobrevivientes de cáncer pulmonar. Recientemente, las guías de la American Association for Thoracic Surgery sobre detección y vigilancia del cáncer de pulmón, recomendaron que los sobrevivientes a largo plazo de cáncer pulmonar deberían ser sometidos anualmente a una TC de baja dosis, para detectar nuevas malignidades pulmonares primarias [6].
Varios aspectos de la vigilancia no han sido abordados, hasta donde llega el conocimiento de los autores del este trabajo. Primero, no está claro si la detección y tratamiento más tempranos de la recidiva mejoran necesariamente la sobrevida a largo plazo. Segundo, los efectos negativos de las imágenes de rutina no han sido investigados a gran escala. Una revisión sistemática conducida por Bach y col. [19], analizó 591 citas sobre los beneficios y peligros de la TC de baja dosis. Aunque aproximadamente sólo el 1% de los pacientes tuvo diagnóstico de cáncer pulmonar, aproximadamente el 20% de los pacientes, a través de todos los estudios, tuvo resultados positivos de las pruebas de detección, requiriendo estudios adicionales. Los autores concluyeron que la TC de baja dosis puede ser beneficiosa para los pacientes con riesgo alto, pero que los peligros potenciales de la detección deben ser investigados y factoreados dentro de futuros protocolos de detección.
Las guías actuales para la vigilancia están basadas en series retrospectivas de pacientes tratados por CPNCP, mayormente adenocarcinoma y carcinoma de células escamosas. Comparado con los tipos histológicos más comunes de cáncer de pulmón, los carcinoides difieren en su conducta, tratamiento y pronóstico global. Dada la naturaleza indolente de los carcinoides típicos, se ha sugerido que, en esa cohorte, las resecciones sublobares pueden producir resultados de sobrevida que son similares a aquellos para las resecciones lobares [20]. El rol de la vigilancia en los sobrevivientes de cáncer carcinoide debería ser examinado separadamente del de los pacientes con tipos más agresivos de cáncer de pulmón [21].
En concordancia con series previas sobre tumores carcinoides, los autores de este trabajo hallaron que el carcinoide atípico y el estatus ganglionar linfático predicen tasas más altas de recidiva después de la resección quirúrgica [21-25]. No obstante, a pesar del seguimiento regular después de la operación, la TC de tórax y abdomen superior de rutina, realizada relativamente de manera pobre, detectó sólo 1 de 4 recaídas. La razón para esa tasa baja de detección de la TC de vigilancia puede estar relacionada con la modalidad de imagen y el patrón de recidiva. La radiología del tórax puede no ser lo suficientemente sensible para detectar pequeñas recidivas intratorácicas. Además, las TC realizadas sin contraste endovenoso pueden omitir metástasis hepáticas o adrenales. Dado que la mayoría de las recaídas fueron metástasis a distancia, los estudios por imágenes restringidos al tórax, fallan en detectar cualquier recidiva extratorácica.
Además de la localización, un régimen racional de vigilancia debe tomar también en cuenta el momento de la recidiva y la probabilidad de eventos. El tiempo más largo para la recidiva en esta serie fue mayor de 11 años. Otras series han reportado recidivas a largo plazo hasta 20 años después de la operación [23,26]. A causa de esos hallazgos, algunos autores recomendaron que el seguimiento debe continuar por al menos 20 años [7]. Sin embargo, si las recidivas son raras, la utilidad de las imágenes repetidas durante ese período extendido, es cuestionable.
Otra consideración importante para diseñar un programa de vigilancia apropiado es contrapesar los beneficios de la vigilancia con los potenciales efectos negativos, teniendo en mente la señal de precaución pronunciada por Bach y col. [19], en su revisión sistemática de la TC de detección. Los riesgos potenciales, además de la exposición a la radiación, incluyen ansiedad aumentada del paciente y resultados falso positivos que pueden llevar a pruebas ulteriores, costos amentados, morbilidad aumentada e incluso aumento de la mortalidad por procedimientos invasivos innecesarios. En una serie previa sobre vigilancia en pacientes tratados por CPNCP en estadio temprano, los autores hallaron que un cuarto de los pacientes requirió pruebas adicionales a causa de resultados falso positivos durante la vigilancia [27]. Aunque es difícil evaluar el balance de riesgos y beneficios de la vigilancia en pacientes con tumores carcinoides en un estudio retrospectivo, los pacientes con el riesgo más bajo de recidiva son los menos propensos a beneficiarse con la vigilancia. La relativa inefectividad de la TC de vigilancia para la detección de las recidivas y el hecho de que un cuarto de las recidivas ocurre después de los 6 años, eleva las cuestiones sobre la costo-efectividad de la vigilancia sistemática con imágenes, en el seguimiento de los pacientes con carcinoides.
Sobre la base de la experiencia de la institución en donde se desempeñan los autores del presente estudio, los pacientes con tumores carcinoides completamente resecados y con ganglios negativos, pueden no justificar una vigilancia a largo plazo, dada la tasa muy baja de recidiva en esa cohorte. No obstante, la vigilancia de rutina con TC debería ser realizada en los pacientes tratados por carcinoide atípico o carcinoide típico con compromiso positivo de los ganglios linfáticos. Dado que la TC es más sensible que la radiología de tórax, debería ser usada como la modalidad primaria de vigilancia. La TC de intervalo debería incluir el tórax y el abdomen superior, incluyendo el hígado y las adrenales, y ser realizada con medio de contraste, para ayudar en la evaluación de los órganos sólidos y ganglios mediastinales. Puesto que el número de recidivas diagnosticadas permanece constante en el tiempo, las TC de vigilancia deberían realizarse cada 12 meses.
La vigilancia de las recidivas después de la resección quirúrgica sigue siendo un aspecto importante de la atención del cáncer, con un impacto significativo en la sobrevida, calidad de vida y costos por la atención médica. Los estudios futuros sobre la vigilancia para la recidiva de los carcinoides pulmonares deberían enfocarse sobre varios aspectos específicos de la naturaleza de la enfermedad. Primero, dada la rareza del cáncer carcinoide pulmonar comparado con otros CPNCP, debería hacerse un esfuerzo para estudiar datos agrupados de múltiples instituciones en una escala internacional. La mayoría de las recidivas de los tumores carcinoides son metástasis a distancia. La vigilancia limitada al tórax o incluso al abdomen superior, puede no ser efectiva para detectar la recaída en otras áreas del cuerpo. La efectividad de otras modalidades de imágenes sistemáticamente orientadas, tales como la TEP/TC y exámenes con octreotide, queda por determinarse y es una cuestión abierta para investigación adicional. Finalmente, son necesarios grandes ensayos prospectivos y randomizados, para estudiar el efecto de la vigilancia en la sobrevida, costos y calidad de vida.
Limitaciones
Este estudio está limitado por su naturaleza retrospectiva y el enfoque sobre pacientes tratados en una única institución. Aunque la mayoría de los pacientes fue sometida a vigilancia de rutina con TC, puede haber variabilidad en sus regímenes de seguimiento, dado que no se especificó un protocolo prospectivo. Como en todo estudio retrospectivo, este análisis no fue diseñado para evaluar el efecto de las imágenes de vigilancia sobre la calidad de vida y la sobrevida. No puede o debe establecerse ninguna conclusión sobre el impacto de las imágenes de vigilancia en la sobrevida, porque ese no fue el foco de este estudio.
Resumen
Después de la operación por tumores carcinoides pulmonares, las imágenes de vigilancia fallaron para detectar la mayoría de las recaídas. Las recidivas se desarrollaron raramente en los pacientes con tumores carcinoides típicos con ganglios linfáticos negativos. Debido al bajo riesgo de recidiva y a la poco clara eficacia de las imágenes de vigilancia, las mismas hechas rutinariamente pueden no estar justificadas en esa cohorte. Los estudios futuros deberían enfocarse sobre los efectos de la vigilancia en la sobrevida y resultados orientados al paciente y sobre las estrategias alternativas para el seguimiento.
♦ Comentario y resumen objetivo: Dr. Rodolfo D. Altrudi